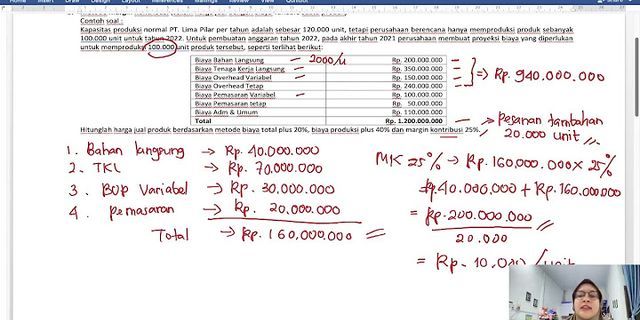
Unduh soal pembahasan Penyetaraan Reaksi Redoks untuk kelas XII SMA/MA
Soal dan pembahasan Penyetaraan Reaksi Reduksi Oksidasi ini dari berbagai penerbit buku seperti Erlangga oleh Michael Purba KTSP 2006 dan Unggul Sudarmo Kurikulum 2013, Yudhistira, Platinum, Grafindo, Phißeta dan Esis
Download File dalam format .doc agar mudah dibaca dan tertata rapi lengkap dengan peta konsep dan prasyarat materi.
Google Drive | Zippyshare | Mirror
(Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba hal. 42)
2 (+1) + S + 3 x (-2) = 0 (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba, 2012 hal. 42)
(+2) + 2 (Cl +2 (-2) ) = 0 (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba, 2012 hal. 42) MnO2 + 2H2SO4 + 2NaI → MnSO4 + Na2SO4 + 2H2O + I2 Yang berperan sebagai oksidator pada reaksi di atas adalah . . . MnO2 + 2H2SO4 + 2NaI → MnSO4 + Na2SO4 + 2H2O + I2 Diketahui bahwa oksidator yang mengalami reduksi atau penurunan biloks. Dimana dilihat bahwa Mn pada MnO2 adalah +4. Biloks Mn pad MnSO4 adalah +2. Terjadi penurunan biloks, sehingga MnO2 menjadi oksidator. (Reaksi Redoks, Soal Ebtanas 2001) aZn + bNO3- → cZn2+ + NH4+ (suasana asam) Jika reaksi diatas disetarakan makan koefisien a, b, dan c berturut-turut adalah . . .
aZn + bNO3- → cZn2+ + NH4+ (suasana asam) 4Zn + NO3- → 4Zn2+ + NH4+
4Zn + NO3- → 4Zn2+ + NH4+ 4Zn + NO3- + 10H+ → 4Zn2+ + NH4+
4Zn + NO3- + 10H+ → 4Zn2+ + NH4+ + 3H2O aZn + bNO3- → cZn2+ + NH4+ 4Zn + NO3- + 10H+ → 4Zn2+ + NH4+ + 3H2O (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba, 2012 hal. 39)
Reaksi asam basa atau garam
(Kumpulan soal persiapan UN 2014 Untuk SMA/MA, tim pemyusun) aI- + SO4-2 → bH2S + cI2 (suasana asam) Jika reaksi tersebut disetarakan maka nilai koefisien a, b dan c adalah . . .
16I- + SO4-2 + 18H+ → H2S + 8I2
16I- + SO4-2 + 18H+ → H2S + 4I2 + 8H2O 16I- + SO4-2 + 18H+ → H2S + 8I2 (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba, 2012 hal. 39) aCl2 + bIO3- → cCl- + IO4- Jika reaksi tersebut disetarakan maka nilai koefisien a, b dan c adalah . . .
Reduksi : Berkurangnya biloks Oksidasi : Bertambah biloksnya
IO3-+ 2OH- → IO4- + H2O + 2e
IO3-+ 2OH- → IO4- + H2O + 2e Cl2 + IO3- + 2OH- → 2Cl- + IO4- + H2O Maka koefesien berturut-turutnya untuk reaksi redoks tersebut adalah : aCl2 + bIO3- → cCl- + IO4- Cl2 + IO3- + 2OH- → 2Cl- + IO4- + H2O (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba hal. 39)
Oksidasi yaitu dimana bertambahnya bilangan oksidasi Maka unsur di atas yang mengalami oksidasi adalah : I- (aq) berubah menjadi I2 (s) Dikarenakan I- = -1 menjadi I2 = 0
Jawaban : (c. I- (aq) berubah menjadi I2 (s) ) (Kimia berbasis eksperimen kelas XII, Penerbit platinum, Sentot Budi Rahardjo, 2012 hal. 85) aCl2 + SO2 + bH2O → SO42- cCl- + dH+ mempunyai nilai koefisien reaksi untuk a, b, c, dan d berturut-turut adalah . . . .
Untuk penyetaraan reaksi dapat menggunakan cara berikut : Menggunakan metode ion elektron
Reduksi : Berkurangnya biloks Oksidasi : Bertambah biloksnya
Karena reaksi berlangsung pada suasana asam maka H2O ditambahkan pada ruas yang kekurangan atom O
SO2 + 2H2O → SO42- + 4H+ + 2e Cl2 + SO2 + 3H2O → 2Cl- + SO4-2 + 4H+ Maka koefesien berturut-turutnya untuk reaksi redoks tersebut adalah : aCl2 + SO2 + bH2O → SO42- cCl- + dH+ Cl2 + SO2 + 2H2O → 2Cl- + SO4-2 + 4H+ Jawaban : (b. 1, 2, 2, 4) (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba hal. 42) aCr2O72- (aq) + bH+ (aq) + cCu+ → dCr3+ (aq) + eH2O (l) + fCu+2 mempunyai harga koefisien reaksi untuk a, b, dan c berturut-turut adalah . . . .
Untuk penyetaraan reaksi dapat menggunakan cara berikut : Menggunakan metode ion elektron
Reduksi : Berkurangnya biloks Oksidasi : Bertambah biloksnya
Karena reaksi berlangsung pada suasana asam maka H2O ditambahkan pada ruas yang kekurangan atom O
Cr2O72- + 14H+ → 2Cr3+ + 7H2O
Cr2O72- + 14H+ → 2Cr3+ + 7H2O
6e + Cr2O72- + 14H+ → 2Cr3+ + 7H2O x1 Cr2O72- + 14H+ + 6Cu+ → 2Cr3+ + 7H2O + 6Cu+2 Maka koefesien berturut-turutnya untuk reaksi redoks tersebut adalah : aCr2O72- (aq) + bH+ (aq) + cCu+ (aq) → dCr3+ (aq) + eH2O (l) + fCu+2 (g) Cr2O72- + 14H+ + 6Cu+ → 2Cr3+ + 7H2O + 6Cu+2 (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba hal. 64) aMnO + bPbO2 + cH+ → dMnO4- + ePb2+ + fH2O mempunyai harga koefisien reaksi untuk a, b, dan c berturut-turut adalah . . . .
Untuk penyetaraan reaksi dapat menggunakan cara berikut : Menggunakan metode ion elektron
Reduksi : Berkurangnya biloks Oksidasi : Bertambah biloksnya
Karena reaksi berlangsung pada suasana asam maka H2O ditambahkan pada ruas yang kekurangan atom O
MnO + 3H2O → MnO4- + 6H+ + 5e PbO2 + 4H+ + 2e → Pb2+ + 2H2O
MnO + 3H2O → MnO4- + 6H+ + 5e x2 PbO2 + 4H+ + 2e → Pb2+ + 2H2O x5 2MnO + 5PbO2 + 8H+ → 2MnO4- + 5Pb2+ + 4H2O Maka koefesien berturut-turutnya untuk reaksi redoks tersebut adalah : aMnO + bPbO2 + cH+ → dMnO4- + ePb2+ + fH2O 2MnO + 5PbO2 + 8H+ → 2MnO4- + 5Pb2+ + 4H2O (Kimia Untuk SMA Kelas XII, Erlangga, Michael Purba hal. 42)
Reaksi Redoks yaitu dimana reaksi yang mengakibatkan ada unsur yang mengalami kenaikan biloks disebut teroksidasi dan yang terjdi penurunan disebut tereduksi. Maka jika dilihat dari soal diatas :
Tidak terjadi reaksi redoks
Jawab : (d. CuO + 2HCl CuCl2 + H2O) (Kumpulan soal persiapan UN 2014 Untuk SMA/MA, tim pemyusun) aCr2O72- (aq) + bC2O42- (aq) + cH+ (aq) → dCr3+ + eCO2 + fH2O mempunyai harga koefisien reaksi untuk a, b, d dan e berturut-turut adalah . . . .
Untuk penyetaraan reaksi dapat menggunakan cara berikut :
aCr2O72- (aq) + bC2O42- (aq) + cH+ (aq) → dCr3+ + eCO2 + fH2O
Cr2O72- + 14H+ → 2Cr3+ + 7H2O
Cr2O72- + 14H+ + 6e → 2Cr3+ + 7H2O (x1) Cr2O72- + 3C2O42- + 14H+ → 2Cr3+ + 7H2O + 6CO2 Maka koefesien berturut-turutnya untuk reaksi redoks tersebut adalah : aCr2O72- (aq) + bC2O42- (aq) + cH+ (aq) → dCr3+ + eCO2 + fH2O Cr2O72- + 3C2O42- + 14H+ → 2Cr3+ + 7H2O + 6CO2 koefisien a, b, d, e berturut-turut adalah 1, 3, 2, 6 Jawaban : (b. 1, 3, 2, 6) (Kumpulan soal persiapan UN 2014 Untuk SMA/MA, tim pemyusun)
Cr2O72- + aH+ + be- → cCr3+ + dH2O Mempunyai harga a, b, c, d berturut-turut . . .
Cr2O72- + 14H+ + be- → 2Cr3+ + 7H2O
Cr2O72- + 14H+ + be- → 2Cr3+ + 7H2O Cr2O72- + 14H+ + 6e- → 2Cr3+ + 7H2O Jawaban : (a. 14, 6, 2, 7) (Kumpulan soal persiapan UN 2014 Untuk SMA/MA, tim pemyusun)
(Jalan Pintas Pintar Kimia:Sumarjo.ANDI. 2010.hal 150)
(Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 150)
BO Min = nomor golongan -8
(Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 151)
Cr2O72- + 14H + 6e- → 2Cr3+ + 7H2O Cr2O72- + 6Br- + 14H+ → 2Cr3+ + 3Br2 + 7H2O (Kimia Berbasis Eksperimen 3.Setot Budi Rahardjo.Platinum.hal 86)
Persamaan ½ reaksi reduksi disetarakan: 8H+ + MnO4-1 + 5e → Mn2+ + 4H2O Setiap 1 mol MnO4-1 menerima 5 mol elektron. BO=+7 → +2 (reduksi 5:menerima 5e) (Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 155) 3Br(g) + a OH-(aq) → b BrO3- + c Br-(aq) + d H2O(l) Harga koefisien a,b,c, dan d supaya reaksi diatas setara adalah . . . .
Sumber: Kimia 3: Parning, Horale & Tiopan.Yudhistira.hal 77 3Br(g) + OH-(aq) → BrO3- + Br-(aq) + H2O(l) Tentukan biloks dari masing-masing unsur 3Br(g) + OH-(aq) → BrO3- + Br-(aq) + H2O(l) Setarakan biloks dari masing-masing unsur 6Br(g) + 6 OH-(aq) → BrO3- + 5 Br-(aq) + 3H2O(l) Jadi, a=6, b=1, c=5, dan d=3
Sumber: Jalan Pintas Pintar Kimia:Sumarjo.ANDI.hal 153 Reaksi autoredoks adalah reaksi redoks dimana reduktor dan oksidasinya sama, yaitu: Cl mengalami reduksi dan oksidasi, sehingga bertindak sebagai reduktor maupun oksidator.
Sumber: Kimia Berbasis Eksperimen 3.Setot Budi Rahardjo.Platinum.hal 86 Persamaan reaksi disetarakan menjadi 6Fe2+ + Cr2O72- + 14H+ → Fe3+ + 2Cr3+ +7H2O Sesuai perbandingan koefisien reaksi: Jumlah mol Fe3+ = 6 × mol Cr2O72- (Kimia Berbasis Eksperimen 3.Setot Budi Rahardjo.Platinum.hal 86)
MnO2 (s) + 4H+ (aq) + 2Cl- (aq) → Mn2+ (aq) + 2H2O (l) + Cl2 (g)
(Kimia untuk kelas 3. Michael Purba. Erlangga.2006.hal 64)
Ciri dari reaksi redoks adalah ada perubahan bilangan oksidasi. (Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 152)
Terlihat pada Cu terjadi perubahan biloks sebesar 2, dan pada N sebesar 3. Samakan banyaknya perubahan itu, kalikan masing-masing dengan bilangan pengali tertentu. Misal 3 akan kita kali 2, sementara 2 akan kita kali 3, jadi perubahannya sama yaitu 6. Tempatkan bilangan pengali tadi di depan Cu dan N Berikutnya setarakan jumlah muatan kiri dan kanan. Di kanan muatannya 3 x (+2) = +6. Agar sama Tambahkan 8 di depan H+ sebelah kiri, sehingga muatan kiri = (−2) + 8 = +6 juga. Terakhir samakan jumlah O.
3Cu + 2NO3- + 8H+ → 3Cu2+ + 2NO + 4H2O Dengan menambah 4 di depan H2O jumlah O kiri 2 x 3 = 6, dan O di kanan (2 + 4) = 6 juga.
Terlihat: (Kimia 3: Parning, Horale & Tiopan.Yudhistira.hal 77)
3As + 5NO3- +4OH- → 3AsO43- + 5NO + 2H2O adalah . . . . Oksidasi: 3As + 24OH-1 → 3AsO43- + 2H2O +15e Reduksi: 15e + 10H2O +5NO3 - → 5NO + 20OH-1 Elektron yang terlibat adalah 15 (Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 155)
Ion PO43- mempunyai bilanga oksidasi -3 -3 = (bilangan oksidasi P) + (4 × bilangan oksidasi O) -3 = P + [4 × (-2)] → P = +5 Jadi, bilangan oksidasi P adalah +5 (Kimia 3: Parning, Horale & Tiopan.Yudhistira.hal 34)
Oksidator adalah yang mengalami reduksi atau penurunan biloks.
(Jalan Pintas Pintar Kimia:Sumarjo.ANDI.2010.hal 150)
MnO4- (aq) + H2C2O4 (aq) + H+ (aq) → Mn2+ (aq) + CO2 (g) + H2O (l) Reaksi setara dari reaksi diatas adalah….
MnO4- (aq) + H2C2O4 (aq) → Mn2+ (aq) + CO2 (g) (suasana larutan asam) Langkah 1: menuliskan kerangka dasar reaksi MnO4- (aq) + H2C2O4 (aq) → Mn2+ (aq) + CO2 (g) Langkah 2 : menyetarakan unsure yang mengalami perubahan bilangan oksidasi dengan member koefisien yang sesuai MnO4- (aq) + H2C2O4 (aq) → Mn2+ (aq) + 2 CO2 (g) Langkah 3 : menentukan jumlah penurunan bilangan oksidasi dari reduktor MnO4- (aq) + H2C2O4 (aq) → Mn2+ (aq) + 2 CO2 (g) Langkah 4 : menyamakan jumlah perubahan bilangan oksidasi tersebut dengan member koefisien yang sesuai MnO4- (aq) + H2C2O4 (aq) → Mn2+ (aq) + 2 CO2 (g) Hasilnya sebagai berikut: 2 MnO4- (aq) + 5 H2C2O4 (aq) → 2 Mn2+ (aq) + 10 CO2 (g) Langkah 5 : menyamakan muatan dengan menambahkan ion H+ 2 MnO4- (aq) + 5 H2C2O4 (aq) + 6 H+ (aq) → 2 Mn2+ (aq) + 10 CO2 (g) (muatan setara) Langkah 6 : menyetarakan atom H dengan menambahkan molekul H2O 2 MnO4- (aq) + 5 H2C2O4 (aq) + 6 H+ (aq) → 2 Mn2+ (aq) + 10 CO2 (g) + 8 H2O (l) (reaksi setara) (KIMIA untuk SMA kelas XII, Michael Purba, Erlangga, 2013, Hlm.45) Cr2O72- (aq) + Fe2+ (aq) + H+ (aq) → H+ (aq) + Cr3+ (aq) + H2O (l) + Fe3+ (aq) Setelah disetarakan, perbandingan koefisien reaksi Cr2O72- : Fe2+ adalah…..
Cr2O72- (aq) + Fe2+ (aq) + H+ (aq) → H+ (aq) + Cr3+ (aq) + H2O (l) + Fe3+ (aq) Disetarakan dengan cara setengah reaksi. Reduksi : 6 e + 14H+ + Cr2O72- → 2Cr3+ + 7H2O Oksidasi : 6 Fe2+ → 6 Fe3+ + 6e- Perbandingan koefisien reaksi Cr2O72- dan Fe2+ adalah 1 : 6 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 402)
aMnO4- + 6 H+ + bH2C2O4 → aMn2+ + 8H2O + 10CO2 a dan b berturut-turut adalah…..
MnO4- + H2C2O4 → Mn2+ + 2CO2 2 MnO4- + 5H2C2O4 → 2Mn2+ + 10CO2 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 357)
a Cr2O7 (aq) + 14 HCl (aq) → b CrCl2 (aq) + c Cl2 (aq) + d H2O (l) Setelah disetarakan, nilai koefisien reaksi a, b, c, dan d secara berurutan adalah…
Cr2O72- + 2Cl- → 2Cr3+ + Cl2 Cr2O72- + 6Cl- → 2Cr3+ + 3Cl2 Ditambah H+ dan H2O untuk menyetarakan H dan O, menjadi: Cr2O72- + 6Cl- + 14 H+ → 2Cr3+ + 3Cl2 + 7 H2O Jadi a = 1, b = 2, c = 3, d = 7 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 403)
aCr2O72- + AsO33- + b H+ → c Cr3+ + AsO43- + d H2O Jika disetarakan, maka harga b, c, dan d dari reaksi tersebut berturut-turut adalah…
Diketahui : aCr2O72- + AsO33- + b H+ → c Cr3+ + AsO43- + d H2O Ditanya : harga b, c, dan d?
aCr2O72- + AsO33- + b H+ → c Cr3+ + AsO43- + d H2O
Cr2O72- + 3 AsO33- + b H+ → 2 Cr3+ + 3 AsO43- + d H2O
Cr2O72- + 3 AsO33- + b H+ → muatan: -2 + 3 (-3) = -11 2 Cr3+ + 3 AsO43- + d H2O → muatan : +6 + 3(-3) = -3
Cr2O72- + 3 AsO33- + 8H+ → 2 Cr3+ + 3 AsO43- + 4H2O (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 512) aCl2 + b OH- → c Cl- + ClO3- + d H2O Harga koefisien a, b, c dan d adalah….
a Cl2 + b OH- → c Cl- + ClO3- + d H2O Tambahkan 6 OH- menyetarakan muatan, sehingga menjadi: 3 Cl2 + 6 OH- → 5 Cl- + ClO3- Tambahkan H2O untuk menyamakan jumlah atom H. 3 Cl2 + 6 OH- → 5 Cl- + ClO3- + 3 H2O (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 322)
aNaIO3 + b NaHSO3 → c NaHSO4 + 2 Na2SO4 + H2O + I2 koefisien reaksi yang tepat untuk a, b, dan c adalah….
2 IO3- + SO32- → SO42- + I2 Dengan demikian, 2 NaIO3 + 5 NaHSO3 → 3 NaHSO4 + 2 Na2SO4 + H2O + I2 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 42)
8 Al + 3 NaNO3 + 5 NaOH + 2 H2O → 8 NaAlO2 + 3 NH3 Zat yan bertindak sebagai oksidator adalah… 8 Al + 3 NaNO3 + 5 NaOH + 2 H2O → 8 NaAlO2 + 3 NH3 Oksidator merupakan zat yang mengalami reduksi, maka dalam reaksi diatas zat yang bertindak sebagai oksidator adalah NaNO3. NO3- → NH3 (mengalami reduksi) (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 49) Br2 + 2NaOH → NaBr + NaBrO + H2O Zat yang mengalami reaksi disproposionasi (autoredoks) berikut perubahan bilangan oksidasinya adalah…
Autoredoks atau disproporsionasi adalah reaksi dimana melibatkan suatu zat yang mengalami reaksi oksidasi sekaligus reduksi. Br2 + 2NaOH → NaBr + NaBrO + H2O Yang mengalami reaksi disproporsionasi adalah bromine dari biloks 0 menjadi -1 dan +1 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 54)
Reaksi oksidasi terdapat pada nomor….
Jadi, reaksi oksidasi terdapat pada nomor 1 ditandai dengan adanya pengikatan oksigen dan 4 ditandai dengan adanya kenaikan biloks dari +5 menjadi +7. (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 58)
NaCl (aq) + a H2O (l) → b Cl2 (g) + c H2 (g) + d NaOH (aq) Harga koefisien a, b, dan c berturut-turut adalah…
Reaksi NaCl + a H2O → b Cl2 + c H2 + d NaOH 2NaCl + 2H2O → 1 Cl2 + 1 H2 + 2 NaOH Harga koefisien a, b dan c adalah 2, 1, dan 1 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 77)
Ada unsure bebas pasti : reaksi redoks Reaksi (a) ada unsure bebas N2 Reaksi (b) tidak ada unsure bebas Reaksi (c) ada unsure bebas Cl2 Reaksi (d) ada unsure bebas Cu Reaksi (e) tidak ada unsure bebas Anda cukup cek jawaban B dan E, missal anda lihat pada pilihan E. 3CH3CHOHCH3 + 2 CrO3 → 3CH3COCH3 + 2 Cr(OH)3 → (redoks) Biloks Cr berubah +6 menjadi +3 (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 86)
Turun 5 (= menangkap 5 elektron) (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 146)
Fe2+ + Cr2O72- → Fe3+ + 2 Cr3+ 6Fe2+ + Cr2O72- → Fe3+ + 2 Cr3+ Fe2+ = 6/1 x 1 mol = 6 mol (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 203)
Ada unsure bebas pasti : reaksi redoks Reaksi (1) ada unsure bebas I2 Reaksi (2) ada unsure bebas H2 , Cl2 Reaksi (3) ada unsure bebas C , Cu Reaksi (4) tidak ada unsure bebas Jawaban : A ( 1, 2, dan 3) (Tip & Trik KIMIA untuk Kelas 1, 2 dan 3 SMA, M.Hasyim Ashari, Erlangga, 2006, Hlm. 312) Sumber : http://kimia.space
Kumpulan Soal dan Pembahasan Sifat Koligatif Larutan Unduh soal pembahasan Sifat Koligatif Larutan untuk kelas XII SMA/MA Soal dan pembahasan Sifat Koligatif Larutan ini dari berbagai penerbit buku seperti Erlangga oleh Michael Purba KTSP 2006 dan Unggul Sudarmo Kurikulum 2013, Yudhistira, Platinum, Grafindo, Phißeta dan Esis Download File dalam format .doc agar mudah dibaca dan tertata rapi lengkap dengan peta konsep dan prasyarat materi. Google Drive | Zippyshare | Mirror Soal dan Pembahasan Sifat koligatif larutan adalah sifat yang bergantung pada …. Jenis zat terlarut Jenis zat pelaut Jumlah zat pelarut Jumlah zat terlarut Konsentrasi larutan JAWABAN : D PEMBAHASAN Sifat koligatif larutan adalah sifat-sifat yang hanya tergantung pada Jumlah (kuantitas) partikel zat terlarut dalam larutan dan tidak bergantung pada jenis atau identitas partikel zat terlarut, tida
Buku Kimia Dasar I untuk Universitas Inilah beberapa Kumpulan Buku Kimia dasar I dapat anda download disini. dan tersedia dalam bahasa Indonesia Maupun English Download Buku Versi Indonesia : Download Buku Versi Indonesia : Kimia Dasar I Dirrectlink | Drive Pengantar Kimia (Kimia Dasar I) Google Drive | Zippyshare Download Buku Versi English : AP Chemistry For Dummies – P. Mikulecky, et al., (Wiley, 2009) WW Drive Google | Dirrect Kimia Dasar I oleh Raymond Chang Dirrect Link Semoga Bermanfaat buat Anda NB : - Cara Download Tunggu Selama 5 Detik Kemudian Klik Skip di Pojok Kanan - Jika Link Download Buku tidak aktif lagi silahkan PM Admin di email maupun difacebook facebook.com/shirosora Tag : belajar kimia dasar, buku kimia dasar, dasar teori kimia, dasar teori reaksi kimia, download buku kimia dasar, ebook kimia dasar, hukum dasar ilmu kimia, hukum dasar kimia, hukum dasar kimia ppt, ilmu dasar kimia, ilmu kimia |

Pos Terkait
Periklanan
BERITA TERKINI
Periklanan
Terpopuler
Periklanan
Tentang Kami
Dukungan

Copyright © 2024 berikutyang Inc.