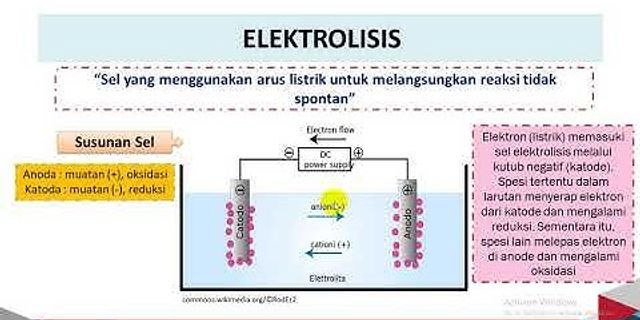
Loading Preview Show Sorry, preview is currently unavailable. You can download the paper by clicking the button above. (1) Laporan KimiaElektrolisisOLEH:Jonathan Naaman XII IPA 3 - 17Regina Fortunata XII IPA 3 -SMA Santo Yakobus(2)I.Tujuan PercobaanUntuk mempelajari perubahan yang terjadi pada elektrolisis larutan garam K2SO4 dan Cu SO4 II. Dasar TeoriBila pada larutan elektrolit diberikan arus listrik searah, maka akan terjadi penguraian pada elektrolit tersebut. Peristiwa ini terjadi pada elektrolisis, tempat berlangsungnya proses ini disebut sel elektrolisis. Sel ini terdiri atas larutan elektrolit, elektroda positif dan elektroda negatif. Pada elektroda negatif (Katoda) terjadi reaksi reduksi, ion-ion positif (Kation) dalam larutan ditarik oleh katoda. Sedangkan pada elektroda negatif (Anoda) terjadi reaksi oksidasi, ion-ion negatif (Anion) dalam larutan ditarik oleh anoda. Reaksi Redoks yang terjadi dipengaruhi oleh jenis elektroda dan jenis anion. Proses elektrolisis digunakan pada penyepuhan, pemurnian logam, dan pembuatan beberapa senyawa seperti NaOH, Cl2 dll. III. Alat dan Bahan- Tabung U - Larutan 0,1M - Elektrode Karbon - Aquades 250 ml - Catu daya - Indikator Universal - Jepit buaya - Gelas kimia - Statif dan Klem IV. Cara Kerja(3)b. Elektrolisis larutan Buat larutan 1 dengan melarutkan garam dengan 250 ml aquades hingga menjadi 0,1 Molar. Tuangkan larutan ini ke dalam tabung U sampai 1,5 cm dari mulut tabung. Celupkan elektrode karbon ke dalam masing-masing kaki tabung U. Hubungkan kedua elektrode dengan sumber arus searah 9 V selama beberapa menit. Setelah terlihat terjadi reaksi angkat elektrode dengan hati-hati. Pipet Fenolftalein/amilum atau menggunakan lakmus / indikator universal, amati perubahan warna yang terjadi. c. Lakukan langkah a dan b dengan larutan 2. d. Dan catat hasilnya ke dalam tabel V. Hasil Pengamatan a. Elektrolisis larutan K2SO4 Hasil Pengamatan elektrolisis K2SO4 Cairan di Reaksi dielektrolisis Hasil di ujidengan Hasil yang terjadi. . Katode 2H20 + 2e- 2OH- +H2 PP 2OH- dan H2 b. Elektrolisis larutan CuSO4 Hasil Pengamatan elektrolisis larutan CuSO4 Cairan di Reaksi Elektrolisis Hasil di ujidengan Hasil yang terjadi (4)VI. Kesimpulana. Elektrolisis adalah penguraian suatu elektrolit oleh arus listrik. Pada sel elektrolisis, reaksi kimia akan terjadi jika arus listrik dialirkan melalui larutan elektrolit, yaitu dari energi listrik (arus listrik) diubah menjadi energi kimia (reaksi redoks). b. Elektrolisis larutan kalium sulfat (K2SO4) pada katoda mengasilkan H2 dan OH - sedangkan pada anoda menghasilkan gas O 2 dan ion 4H+. c. Elektrolisis larutan tembaga (II) sullfat (CuSO4) pada katoda menghasilkan (5)Laporan FisikaOLEH:Jonathan Naaman XII IPA 3 - 17SMA Santo YakobusJawabannya B. Perhatikan ionisasi larutan kalium sulfat K₂SO₄ berikut ini: K₂SO₄(aq) → 2K⁺(aq) + SO₄²⁻(aq) Pada katoda, terjadi persaingan antara air dan ion K⁺. Berdasarkan nilai potensial reduksi (E⁰), maka air yang akan tereduksi di katoda. Sementara itu, terjadi persaingan antara ion SO₄²⁻ dengan air di anoda. Oleh karena bilangan oksidasi S pada SO₄²⁻ telah mencapai +6 atau dikatakan keadaan maksimum, maka SO₄²⁻ tidak dapat mengalami oksidasi. Sehingga, pelarut air yang akan teroksidasi di anoda Singkatnya, ⇒ Ingat, kation K⁺ termasuk logam aktif golongan IA sehingga pelarut air yang akan mengalami reduksi di katoda. ⇒ Sedangkan anion SO₄²⁻ merupakan sisa asam oksi sehingga pelarut air yang akan teroksidasi di anoda. Katoda : 2H₂O(l) + 2e → H₂(g) + 2OH⁻(aq).......(kalikan 2) Anoda : 2H₂O(l) → O₂(g) + 4H⁺(aq) + 4e Menjadi, Katoda : 4H₂O(l) + 4e → 2H₂(g) + 4OH⁻(aq) Anoda : 2H₂O(l) → O₂(g) + 4H⁺(aq) + 4e Campuran yang menghasilkan garam terhidrolisis sebagian dan bersifat basa adalah a. 100 mL larutan NaOH 0, 2M + 100 mL larutan CH3COOH 0,4 M b. 50 mL … tolong di jawab dong kak besok di kumpulin Pernyataan yg tepat mengenai asam lakmus ditunjukan oleh nomer Pernyataan yg tepat mengenai asam lakmus ditunjukan oleh nomer Campuran yang menghasilkan garam terhidrolisis sebagian dan bersifat basa adalaha. 100 mL larutan NaOH 0, 2M + 100 mL larutan CH3COOH 0,4 M b. 50 mL l … soal pilihan ganda Alat yang digunakan untuk mengukur masa eletron adalah Argon adalah gas inert yang digunakan dalam bola lampu untuk memperlambat penguapanfilamen. Sebuah bola lampu tertentu yang mengandung argon pada 1,20 … Tuliskan Rumus Isomer dari a, b dan C Tentukan pH campuran 150 mL NH40H 0,2 M Kb NH+OH 1 x 10-5 dengan 150 HCI 0.1 M? Reaksi antara 100 mL CH;COOH 0,01 M dengan 100 mL CH,COONa 0,02M, jika Ka CH3COOH I x 105, hitunglah pH penyangga larutan tersebut? Campuran yang menghasilkan garam terhidrolisis sebagian dan bersifat basa adalah a. 100 mL larutan NaOH 0, 2M + 100 mL larutan CH3COOH 0,4 M b. 50 mL … tolong di jawab dong kak besok di kumpulin Pernyataan yg tepat mengenai asam lakmus ditunjukan oleh nomer Pernyataan yg tepat mengenai asam lakmus ditunjukan oleh nomer Campuran yang menghasilkan garam terhidrolisis sebagian dan bersifat basa adalaha. 100 mL larutan NaOH 0, 2M + 100 mL larutan CH3COOH 0,4 M b. 50 mL l … soal pilihan ganda Alat yang digunakan untuk mengukur masa eletron adalah Argon adalah gas inert yang digunakan dalam bola lampu untuk memperlambat penguapanfilamen. Sebuah bola lampu tertentu yang mengandung argon pada 1,20 … Tuliskan Rumus Isomer dari a, b dan C Tentukan pH campuran 150 mL NH40H 0,2 M Kb NH+OH 1 x 10-5 dengan 150 HCI 0.1 M? Reaksi antara 100 mL CH;COOH 0,01 M dengan 100 mL CH,COONa 0,02M, jika Ka CH3COOH I x 105, hitunglah pH penyangga larutan tersebut? |

Pos Terkait
Periklanan
BERITA TERKINI
Periklanan
Terpopuler
Periklanan
Tentang Kami
Dukungan

Copyright © 2024 berikutyang Inc.